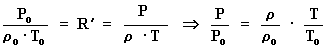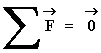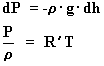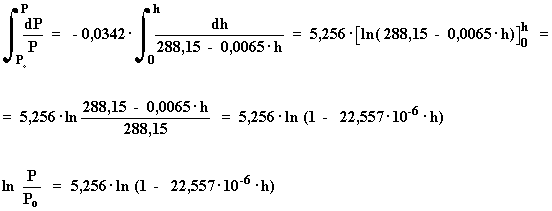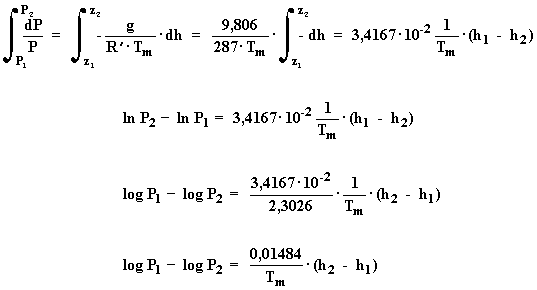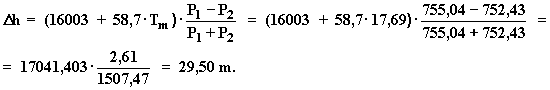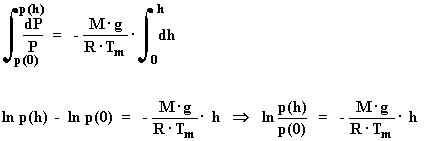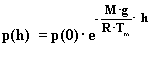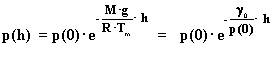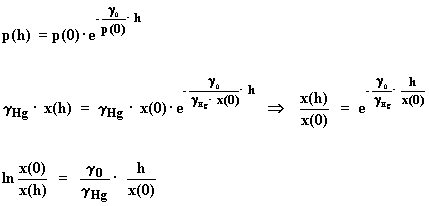1. La ley de los gases ideales aplicada a la atmósfera.
Consideremos una masa gaseosa de volumen V que se encuentra a una presión
P y una temperatura absoluta T.
La ley de los gases ideales establece que [1]:
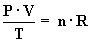
En donde:
P: presión del gas.
V: volumen del gas.
T: temperatura absoluta del gas (º K).
n: es el número de moles del gas.
R: constante universal de los gases ideales.
Sea m la masa total de gas que ocupa el volumen V y M el peso de cada
mol o peso molecular, entonces se verifica que:
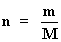
Sustituyendo en [1]:
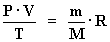
La definición de densidad ( r
):
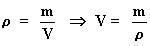
Sustituyendo:
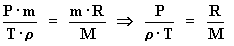
Sea:
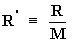
Por lo tanto:
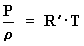
Para el caso del aire:
M = 28,9644 g / mol.
R' = 2,87 · 106 ergios/(g ºK) = 287 julios /(kg.
ºK)
Si llamamos Po, r o, y To a las condiciones
del aire de la atmósfera a nivel del mar:
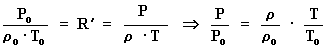
Donde:
Po = 1 atm = 760 mm de Hg = 1013,25 milibares = 1013 HPa = 29,9212 in
Hg.
r o = 1,225 Kg / m3
= 0,001225 g / cm3 .
To = 288,15 º K (15 ºC).
Definamos los parámetros que siguen:
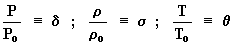
La ecuación queda:
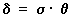
2. Ecuación fundamental de la presión hidrostática.
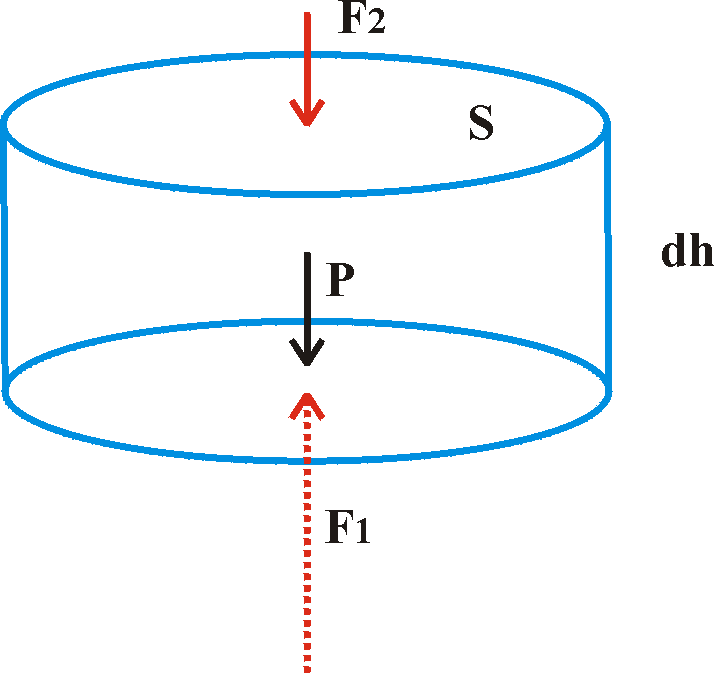
Consideremos dentro de un fluido en equilibrio una porción cilíndrica
del mismo, de altura dh y sección transversal S (ver figura 1).
La suma de todas las fuerzas que actúan sobre la porción
cilindrica es cero. Por razones de simetría las fuerzas sobre las
paredes laterales del cilindro se anulan unas a otras, dando la resultante
nula. En la dirección vertical existe hacia arriba la fuerza ejercida
por la presión p de valor F1 = p S y hacia abajo la que
ejerce p + dp, de valor F2 = (p + dp) S.
El peso de la porción cilindrica definida es:
P = m · g
Como el fluido esta en equilibrio:
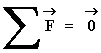
Luego:
F1 - F2 - P = 0
p·S - (p + dp)·S - m · g = 0
p·S - (p + dp)·S - r ·V
· g = 0
p·S - (p + dp)·S - S · dh · r
· g = 0
Simplificando:
dP = - r g dh
El signo negativo indica que la presión disminuye conforme aumenta
la altitud.
3. Ecuación de la presión en función
de la altitud para la atmósfera tipo
La atmósfera tipo o estándar es aquella que tiene definido
unos valores fijos de presión, densidad y temperatura a nivel del
mar y se rige por la ley de los gases ideales y la ecuación de la
presión hidrostática.
Tomemos las ecuaciones [2] y [4]:
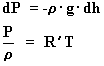
Eliminando la densidad:
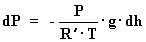
Se considera que para alturas inferiores a 11 Km, la temperatura varía
con la altitud a razón de 6,5 ºC por Km:
T = 288,15 - 0,0065 h ( T en ºK y h en metros)
Por lo tanto:
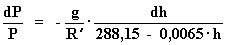
Integrando para h = 0 implica P = Po y sustituyendo los valores g =
9,806 m/ s2 y R' = 287 julios /(kg. ºK):
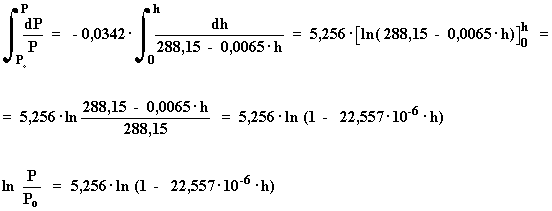
Luego:
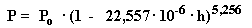
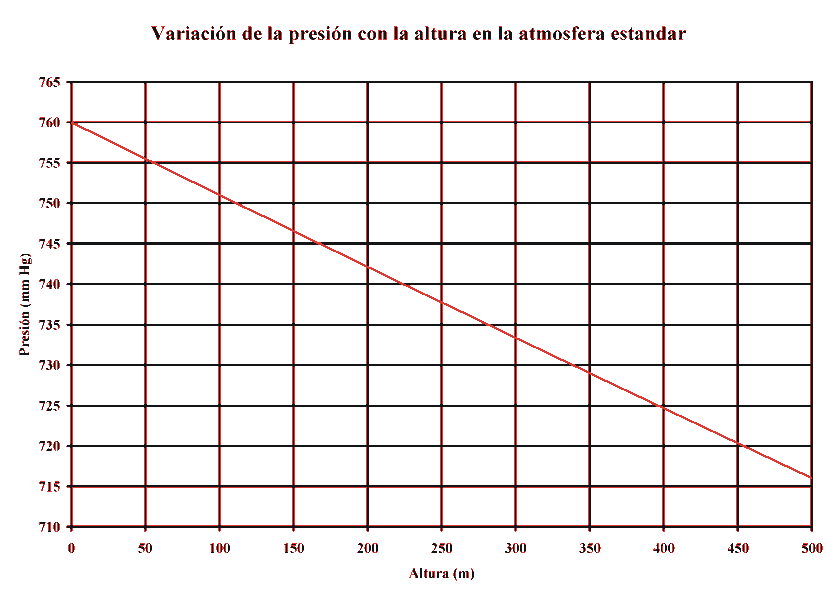
Representando esta variación de la presión con la altura,
en la troposfera, es decir, entre los 0 y 11.000 metros:
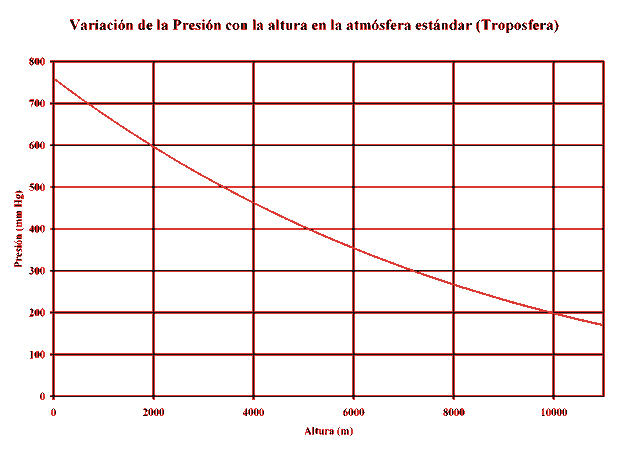
Si consideramos la variación en los primeros 500 metros, la curva
se confunde prácticamente con una recta:
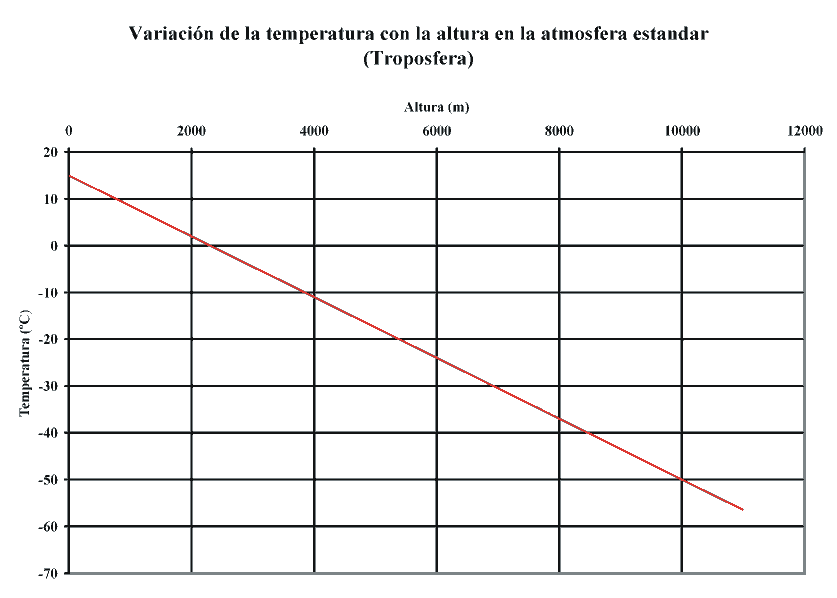
Las gráficas de variación de la temperatura con la altitud
son:
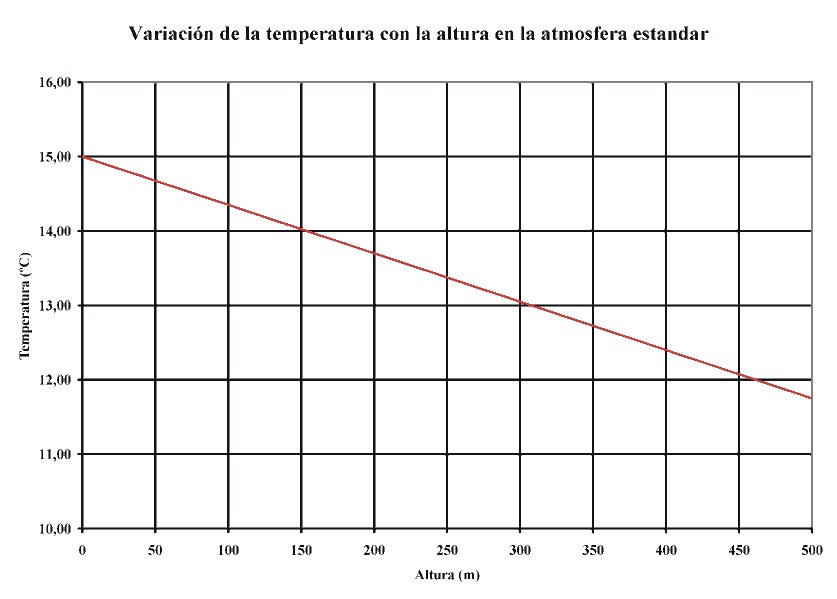
En los primeros 500 metros:
4. Formula de nivelación barométrica
Si conocemos la presión y la temperatura en dos puntos separados
por una altura D h, podemos hallar una ecuación
que nos calcule esta diferencia de altitud.
Partamos de la expresión [5]:
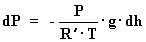
Podemos considerar que la temperatura de la masa de aire existente entre
los dos puntos es igual a la temperatura media entre los mismos, es decir:
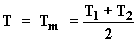
Luego:
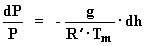
Integrando y sustituyendo los valores de las constantes g = 9,806 m/
s2
y R' = 287 julios /(kg. ºK):
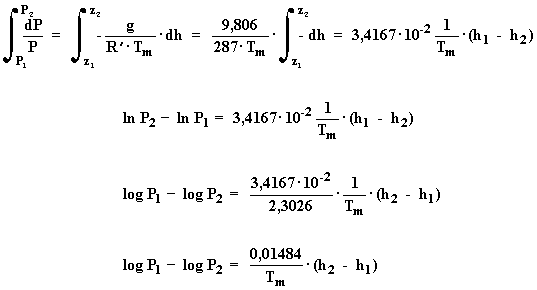
Luego:
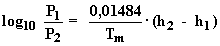
Luego la diferencia de cota (D h = h2
- h1) entre el punto 1 y 2, es:
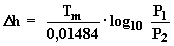
Tm en ºK y D h en metros.
Para alturas inferiores a 500 m, se puede emplear la siguiente fórmula,
que al no aparecer la función logarítmica facilita los cálculos:
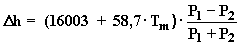
Tm en ºC y D h en metros.
Ejemplo I:
Queremos medir la altura de un edificio de 11 plantas, para lo cual
se toman dos medidas de presión y temperatura, una en la planta
baja y la otra en la planta undécima. Las lecturas nos han dado:
| |
Temperatura
|
Presión
|
| Planta 0 |
19,79 º C
|
755,04 mm de Hg
|
| Planta 11 |
15,59 º C
|
752,43 mm de Hg
|
Calcular la diferencia de cota entre los dos puntos.
Emplearemos las dos formulas:
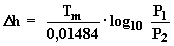
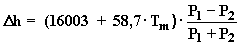
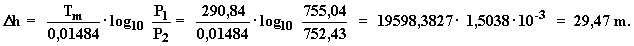
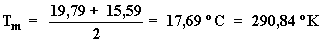
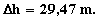
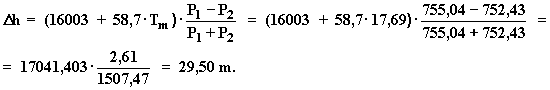
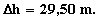
5. Fórmula barométrica de Edmund Halley
(1656 - 1742).
En 1686, en un comunicado a la Royal Society de Londres, el astrónomo
Edmund Halley estableció la fórmula exponencial de variación
de la presión con la altura a temperatura constante.
Partamos de la expresión [5]::
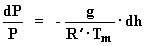
Recordando que:
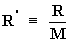
Luego:
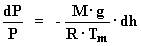
Integrando:
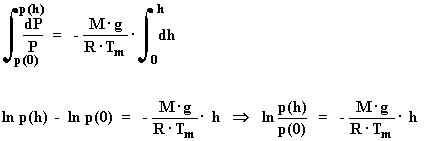
Despejando p(h) nos da la fórmula de la variación de la
presión con la altura:
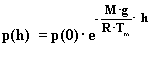
La fórmula que daba la variación de la densidad con la
presión tenía la siguiente expresión:
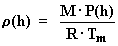
El peso especifico del aire U o a la cota
cero es:
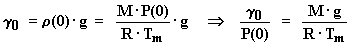
Sustituyendo en la expresión exponencial:
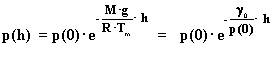
La presión a la altura h será igual al peso especifico
del mercurio multiplicado por la altura de la columna del barómetro
de mercurio a la cota h:
p(h) = U Hg · x(h)
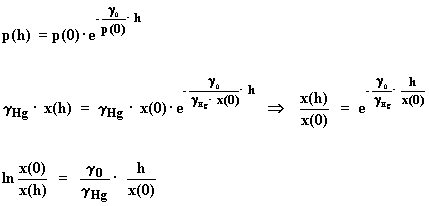
Luego:
Despejando h:
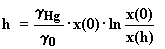
Según Halley la relación entre el peso especifico del
aire a cota cero y el peso especifico del mercurio es:
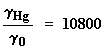
Luego la expresión final es:
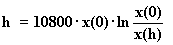
Ejemplo II:
Queremos medir la altura de un edificio de 11 plantas, para lo cual
se toman dos medidas de presión, una en la planta baja y la otra
en la planta undécima. Las lecturas nos han dado:
| |
x(h)
|
| Planta 0 |
755,04 mm de Hg
|
| Planta 11 |
752,43 mm de Hg
|
Calcular la diferencia de cota entre los dos puntos, empleando la fórmula
de Halley.
Sustituimos en la fórmula:
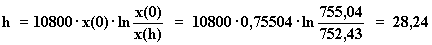
Luego:
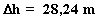
6. Bibliografía
ISIDORO CARMONA, A. (1996), Aerodinámica y actuaciones del
avión, Madrid, Editorial Paraninfo, pp. 19 - 43.
BERBERAN, N.M.;BODUNOV, E.N.;POGLIANI, L. (1997), On barometric formula,
Am. J. Phys., 65 (5), pp. 404 - 12
PITA SUAREZ-COBIAN, P.; LORENTE PEREZ, J.M. (1942), Meteorología
Aeronáutica, Madrid, Saeta. pp. 38- 45
PETTERSSEN, S. (1951) Introducción a la meteorología,
Buenos Aires, Espasa Calpe Argentina, S.A., pp. 32-3
SYNERGY, R. P. (1994), Kiting to Record Altitudes, Toronto, Write
Publications.
JUAN MIGUEL SUAY BELENGUER
Ingeniero Superior Industrial
D. E. A. en Historia de la Ciencia
jmsb2@alu.ua.es
03 enero 2004
Otros artículos de Física